Một trong những mối quan ngại chính đối với việc sử dụng metformin trong thai kỳ là khả năng qua nhau thai. Nồng độ metformin trong máu cuống rốn dao động từ 50 - 100% so với nồng độ ở mẹ. Metformin là cơ chất của nhiều hệ thống vận chuyển tế bào, trong đó có protein vận chuyển cation hữu cơ (OCT3) được biểu hiện trong mô nhau đóng vai trò chính trong quá trình này. Biểu hiện OCT3 thấp trong tam cá nguyệt đầu và tăng dần theo tuổi thai. Song song đó, vị trí tác động chính của metformin là ty thể thì rất ít và chưa hoàn thiện trong giai đoạn sớm của thai kỳ [1]. Do đó metformin được cho là an toàn khi sử dụng ở giai đoạn sớm của thai kỳ và không làm tăng nguy cơ dị tật bẩm sinh.
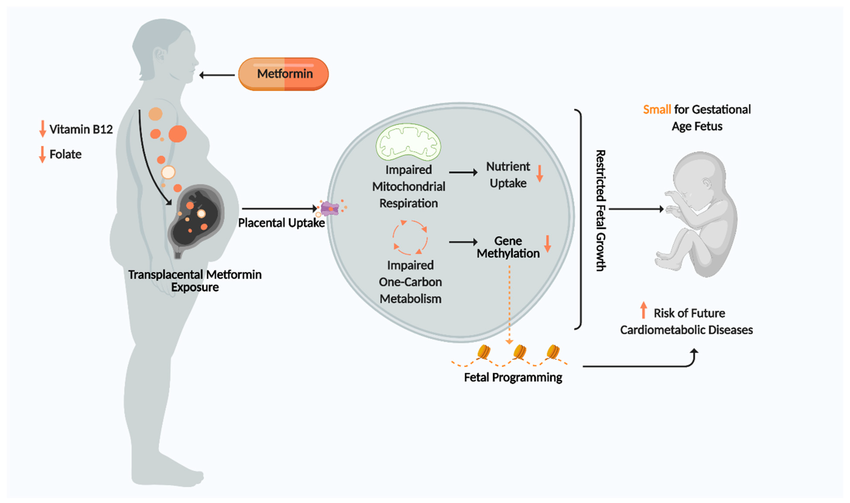
Hình: Cơ chế ảnh hưởng của metformin đến thai nhi
Tuy nhiên, tác động toàn diện của việc sử dụng metformin trong thai kỳ vẫn đang được nghiên cứu làm rõ. Một số bằng chứng cho thấy metformin có thể ảnh hưởng đến sự phát triển thai nhi, sinh khả dụng của dưỡng chất và quá trình lập trình biểu sinh (epigenetic programming) [1-2]. Metformin làm chuyển dịch chuyển hóa tế bào từ trạng thái đồng hóa sang dị hóa, đồng thời ức chế tăng trưởng và giảm vận chuyển các chất dinh dưỡng qua nhau thai (như glucose, acid amin) ngay cả khi môi trường có sẵn dưỡng chất này. Sự thiếu hụt calo trong bào thai có thể giải thích cho xu hướng giảm cân nặng sơ sinh và tăng tỷ lệ thai nhỏ so với tuổi thai khi dùng metformin trong thai kỳ [1-2]. Trạng thái dị hóa và thiếu dưỡng chất có thể tạo ra một môi trường phát triển theo "giả thuyết kiểu hình tiết kiệm" (thrifty hypothesis) – làm tăng nguy cơ mắc bệnh tim mạch – chuyển hóa trong giai đoạn trưởng thành [3].
Tiếp xúc với metformin trước sinh còn làm thay đổi đáng kể biểu hiện gen tại gan. Gen Insulin-induced 1 (Insig-1) có vai trò trong sinh tổng hợp lipid và phát triển mô mỡ được biểu hiện tăng đáng kể (gấp ~3 lần) ở gan chuột đực có mẹ dùng metformin trong thai kỳ; xu hướng tương tự được thấy ở chuột cái nhưng không có ý nghĩa thống kê [4]. Ngoài ra, biểu hiện gen H19 cũng tăng, đây là gen có biểu hiện rất thấp ở gan người trưởng thành nhưng tăng trong đái tháo đường type 2. H19 làm giảm methyl hóa và tăng biểu hiện Hnf4α, từ đó hoạt hóa các gen tạo glucose (gluconeogenesis) sớm hơn bình thường [5].
Một số nghiên cứu cho thấy metformin ảnh hưởng đến sinh khả dụng của các chất cho nhóm methyl như axit folic, vitamin B12, và ảnh hưởng trực tiếp đến chuyển hóa carbon. Kết quả là giảm methyl hóa DNA và thay đổi tín hiệu lập trình biểu sinh trong cơ thể thai nhi [2].
Bảng: Ảnh hưởng của metformin với thai nhi
|
Nghiên cứu
|
Loại NC
|
Chỉ định
|
Nhóm chứng
|
GA
|
PB
|
CA
|
BW
|
MS
|
LGA
|
SGA
|
NH
|
AP-GAR
|
NICU
|
RDS
|
|
Rowan et al. (MiG) [6]
|
RCT
|
GDM
|
Insulin
|
↓
|
↑
|
|
↔
|
|
|
|
↓
|
↔
|
|
↔
|
|
Tertti et al. [20]
|
RCT
|
GDM
|
Insulin
|
↔
|
↔
|
|
↔
|
|
|
|
|
↔
|
↔
|
|
|
Ainuddinn et al. [16]
|
RCT
|
GDM
|
Insulin
|
|
|
|
↓
|
|
↔
|
↔
|
↓
|
↓
|
|
|
|
Balsells et al. [8]
|
SR/MA
|
GDM
|
Insulin
|
↓
|
↑
|
|
↔
|
↔
|
↔
|
↔
|
↔a
|
↔
|
↔
|
↔
|
|
Guo et al. [7]
|
SR/MA
|
GDM
|
Insulin
|
↓
|
↔
|
↔
|
↓
|
↓
|
↔
|
↔
|
↓
|
↔
|
↓
|
↔
|
|
Tarry-Adkins et al. [15]
|
SR/MA
|
GDM
|
Insulin
|
|
|
|
↓
|
↓
|
↓
|
↔
|
|
|
|
|
|
Feig et al. (MiTy) [17]
|
RCT
|
T2DM
|
Giả dược + insulin
|
↔
|
↔
|
↔
|
↓
|
|
↔
|
↑
|
↔
|
|
|
↔
|
|
Lin et al. [13]
|
Thuần tập
|
T2DM
|
Insulin
|
|
↔
|
↓
|
|
|
↔
|
↔
|
|
↔
|
|
|
|
Løvvik et al. (PregMet2) [9]
|
RCT
|
PCOS
|
Giả dược
|
↔
|
↔
|
|
|
|
|
|
|
|
|
|
|
Zeng et al. [10]
|
SR/MA
|
PCOS
|
Giả dược
|
|
↓
|
|
|
|
|
|
|
|
|
|
|
Given et al. [14]
|
Bệnh chứng
|
PCOS, T2DM
|
Không sử dụng Met
|
|
|
↔
|
|
|
|
|
|
|
|
↓
|
|
Diav-Citrin et al. [12]
|
Thuần tập
|
PCOS, T2DM
|
Insulin
|
|
↔
|
↔
|
|
|
|
|
|
|
|
|
|
Brand et al. [11]
|
Thuần tập
|
PCOS, GDM, T2DM
|
Insulin
|
|
↔
|
↔
|
↓
|
|
↔
|
↑
|
↔
|
|
|
|
Chú thích: BW cân nặng sơ sinh, CA dị tật bẩm sinh, GA tuổi thai tại thời điểm sinh, GDM đái tháo đường thai kỳ, LGA thai lớn hơn tuổi thai, Met metformin, MS thai to, NH hạ đường huyết sơ sinh, NICU khoa hồi sức sơ sinh PB sinh non, PCOS hội chứng buồng trứng đa nang, RCT thử nghiệm lâm sàng ngẫu nhiên có đối chứng, RDS hội chứng suy hô hấp, SGA thai nhỏ so với tuổi thai, SR/MA nghiên cứu tổng quan hệ thống và phân tích gộp, T2DM đái tháo đường typ 2
↑ = tăng có ý nghĩa thống kê
↓ = giảm có ý nghĩa thống kê
↔ = không có sự khác biệt có ý nghĩa thống kê
Tuổi thai / Sinh non
Nhiều nghiên cứu cho thấy việc sử dụng metformin trong điều trị đái tháo đường thai kỳ (GDM) dẫn đến tuổi thai thấp hơn so với nhóm chứng [6-8]. Trong khi đó, Guo và cộng sự không ghi nhận sự khác biệt đáng kể về tỷ lệ sinh non. Ngược lại, ở bệnh nhân đái tháo đường type 2, metformin không có mối liên quan đáng kể đến tuổi thai hoặc sinh non, mặc dù chưa có phân tích gộp nào cho nhóm này [7].
Ngoài ra, sinh non cũng được nghiên cứu ở phụ nữ mắc hội chứng buồng trứng đa nang (PCOS), so sánh việc dùng metformin với giả dược. Kết quả cho thấy nguy cơ sinh non tương tự nhau và metformin có xu hướng tác dụng thúc đẩy việc mang thai đủ tháng [9]. Hơn nữa, một phân tích tổng hợp trên nhóm dân số này cho thấy tỷ lệ sinh non thấp hơn đáng kể ở nhóm dùng metformin [10].
Cuối cùng, nghiên cứu thuần tập của Brand và cộng sự đã đánh giá ảnh hưởng của metformin ở các bệnh nhân GDM, T2DM và PCOS. Trẻ sơ sinh ở các bà mẹ được điều trị kết hợp metformin và insulin có khả năng sinh non cao hơn so với trẻ chỉ tiếp xúc với insulin. Đáng chú ý là tỷ lệ sinh non là tương đương giữa nhóm chỉ dùng metformin và nhóm chỉ dùng insulin [11].
Dị tật bẩm sinh
Khả năng metformin đi qua nhau thai gây nên sự lo ngại về ảnh hưởng của nó đến sự phát triển thai nhi, đặc biệt khi sử dụng trong giai đoạn hình thành cơ quan (tuần thai thứ 4 đến 12). Dữ liệu hiện có về việc sử dụng metformin trong ba tháng đầu thai kỳ còn hạn chế nhưng phần lớn đều cho thấy metformin không làm tăng nguy cơ dị tật bẩm sinh nghiêm trọng so với insulin [12].
Trong một nghiên cứu thuần tập, Lin và cộng sự ghi nhận nguy cơ dị tật bẩm sinh thấp hơn ở phụ nữ mắc T2DM điều trị bằng metformin so với điều trị insulin. Nguyên nhân chưa rõ, nhưng có thể phụ nữ dùng metformin có tình trạng đái tháo đường nhẹ hơn so với nhóm dùng insulin [13]. Một nghiên cứu bệnh-chứng trên 50.167 trẻ sơ sinh phát hiện nguy cơ teo van động mạch phổi cao hơn sau khi phơi nhiễm metformin. Các tác giả cũng khuyến nghị nên có thêm các nghiên cứu giám sát để tăng kích thước mẫu và xác minh kết quả này vì nhiều khả năng đây là phát hiện ngẫu nhiên [14].
Cân nặng sơ sinh/Thai nhỏ so với tuổi thai (SGA)/Thai to so với tuổi thai (LGA)/Thai to (Macrosomia)
Trong phân tích gộp của Guo và Tarry-Adkins, trẻ sơ sinh có mẹ dùng metformin có cân nặng thấp hơn. Ngoài ra, tỷ lệ thai to giảm đáng kể, nhưng không có sự khác biệt về tỷ lệ thai nhỏ so với tuổi thai và thai to so với tuổi thai [7,15].
Về đái tháo đường trước thai kỳ, Ainuddin và cộng sự ghi nhận cân nặng sơ sinh tương đương giữa các nhóm dùng metformin đơn độc, insulin đơn độc và điều trị kết hợp [16]. Nghiên cứu MiTy cho thấy tăng tỷ lệ thai nhỏ so với tuổi thai và giảm tỷ lệ thai to ở nhóm mẹ dùng metformin + insulin so với insulin + giả dược. Tỷ lệ thai to so với tuổi thai là tương đương giữa hai nhóm [17]. Việc sử dụng metformin không ảnh hưởng đến cân nặng sơ sinh ở con của phụ nữ mắc PCOS [9].
Hạ đường huyết sơ sinh
Nhiều nghiên cứu cho thấy metformin giúp giảm nguy cơ hạ đường huyết sơ sinh trong điều trị GDM [6,7,16]. Nghiên cứu thuần tập của Brand và cộng sự cho thấy metformin liên quan đến giảm nguy cơ hạ đường huyết sơ sinh, bất kể chỉ định [11].
Tuy nhiên, Ainuddin và cộng sự không xác nhận tác dụng giảm nguy cơ hạ đường huyết sơ sinh của metformin trong điều trị cho mẹ mắc T2DM [16]. Thử nghiệm MiTy ghi nhận tỷ lệ hạ đường huyết tương đương giữa nhóm insulin + metformin và nhóm insulin + giả dược ở trẻ có mẹ mắc T2DM [17].
Biến chứng sơ sinh khác
Kết luận tổng thể từ nhiều nghiên cứu ngẫu nhiên có đối chứng và phân tích gộp cho thấy metformin không làm tăng tỷ lệ nhập NICU (Khoa Chăm sóc Tích cực Sơ sinh), nguy cơ gây hội chứng suy hô hấp hoặc điểm APGAR (chỉ số đánh giá sức khoẻ trẻ sơ sinh khi mới ra đời) dưới mức bình thường sau 5 phút [6,7,17].
Nghiên cứu ảnh hưởng của metformin đến trẻ trong giai đoạn tiền dậy thì
Con của các bà mẹ mắc GDM trong nghiên cứu MiG được chia thành nhóm tại các trung tâm y tế Adelaide và Auckland để theo dõi ảnh hưởng lâu dài của metformin. Tại Adelaide (metformin: n = 58; insulin: n = 51), người ta ghi nhận không có sự khác biệt về các chỉ số nhân trắc học khi trẻ 2 và 7 tuổi. Ngược lại, tại Auckland (metformin: n = 45; insulin: n = 54), khi trẻ 2 tuổi, người ta nhận thấy nhóm trẻ có mẹ dùng metformin trong thai kỳ có BMI, vòng ngực, vòng cánh tay, vòng eo và hông, tỷ lệ eo/hông và độ dày lớp mỡ dưới da cao hơn đáng kể. Khi 9 tuổi, trẻ vẫn có cân nặng, vòng cánh tay và vòng eo, tỷ lệ vòng eo/chiều cao và khối lượng mỡ ở tay cao hơn. Tuy nhiên, tổng lượng mỡ, mỡ dưới da và nội tạng là tương đương giữa hai nhóm [6].
Các nghiên cứu tương tự ở trẻ có mẹ mắc PCOS, so sánh metformin với giả dược, cho thấy trẻ nhóm giả dược có cân nặng, BMI và tỷ lệ thừa cân/béo phì cao hơn ở tuổi 4, không có khác biệt về chiều cao. Dữ liệu từ nghiên cứu theo dõi PedMet (5–10 tuổi) của nhóm PregMet chỉ ra rằng việc dùng metformin trong thai kỳ liên quan đến tăng BMI, béo phì, vòng eo và tỷ lệ eo/chiều cao, không ảnh hưởng đến chiều cao ở trẻ [18]. Cuối cùng, nghiên cứu thuần tập cả Brand so sánh giữa metformin đơn độc, metformin + insulin và insulin đơn độc không thấy khác biệt về tỷ lệ béo phì hoặc phát triển vận động-xã hội [11].
Mặc dù còn hạn chế dữ liệu, việc mẹ sử dụng metformin trong thai kỳ được cho là có ảnh hưởng tiêu cực đến sức khỏe sinh sản của trẻ. Các nghiên cứu trên động vật cho thấy metformin làm giảm kích thước và sự phát triển tinh hoàn cũng như giảm sản xuất testosterone [19]. Tuy nhiên, không có sự khác biệt về kích thước tinh hoàn ở trẻ từ 33 đến 85 tháng tuổi sinh ra từ các bà mẹ mắc GDM được ngẫu nhiên dùng metformin hoặc insulin [20].
Các hướng dẫn của quốc gia và quốc tế về quản lý tăng đường huyết trong thai kỳ hiện vẫn còn nhiều khác biệt. Hiệp hội Đái tháo đường Hoa Kỳ (ADA) khuyến cáo insulin là lựa chọn điều trị đầu tay, và metformin chỉ được cân nhắc như lựa chọn thứ hai khi cần thiết. Mặc dù vậy, hiện tại ADA cũng xếp metformin vào nhóm B theo phân loại an toàn thuốc dùng trong thai kỳ, đồng thời ghi nhận các bằng chứng về hiệu quả và độ an toàn của metformin từ các thử nghiệm lâm sàng ngẫu nhiên. Mặt khác, ADA khuyến cáo rằng metformin nên được ngưng sau khi kết thúc tam cá nguyệt đầu tiên nếu được sử dụng trước thai kỳ ở phụ nữ mắc PCOS với chỉ định hỗ trợ thụ thai do tăng nguy cơ qua nhau thai hơn [21].
Theo Hiệp hội Đái tháo đường Canada, metformin có thể được sử dụng như một phương án thay thế insulin trong điều trị GDM. Tuy nhiên, bác sĩ cần cung cấp đầy đủ thông tin cho bệnh nhân rằng metformin có khả năng qua nhau thai, dữ liệu về tác động lâu dài trên trẻ vẫn còn hạn chế và khoảng 40% bệnh nhân vẫn cần bổ sung insulin để đạt được mức kiểm soát glucose huyết tối ưu [22].
Viện Y tế và Chất lượng Điều trị Quốc gia Anh (NICE) khuyến nghị rằng metformin là thuốc điều trị đầu tay cho phụ nữ mang thai mắc GDM có chỉ số đường huyết lúc đói nhỏ hơn 7 mmol/l, không kèm theo các biến chứng như thai to hoặc đa ối nếu mục tiêu kiểm soát đường huyết không đạt được sau 1–2 tuần điều chỉnh chế độ ăn và luyện tập [23]. Bên cạnh đó, hướng dẫn điều trị của Mạng lưới Hướng dẫn Liên trường Scotland (SIGN) cho phép cân nhắc metformin hoặc insulin như là lựa chọn điều trị hạ glucose huyết ban đầu ở phụ nữ mắc GDM [24].
Hiện nay tại Việt Nam, insulin là thuốc duy nhất được chấp nhận sử dụng trên phụ nữ mang thai [25].
Tóm lại, metformin sử dụng trong thai kỳ không làm tăng các bất thường bẩm sinh và nhìn chung được dung nạp tốt, rất hiếm gặp các tác dụng không mong muốn nghiêm trọng. Tuy nhiên, việc sử dụng metformin trong thai kỳ vẫn chưa thống nhất giữa các khuyến cáo của các quốc gia, do đó nhân viên y tế cần cân nhắc dựa vào hướng dẫn điều trị của quốc gia và tình trạng của bệnh nhân để đánh giá, cân nhắc việc lựa chọn thuốc kiểm soát đường huyết trong thai kỳ.
Biên soạn: Nguyễn Ngọc Ánh - Đơn vị Dược lâm sàng và thông tin thuôc